Melakukan Eksperimen Miller-Urey
Pelajari lebih lanjut: Penafian PMC | Pemberitahuan Hak Cipta PMC
Abstrak
Pada tahun 1953, Stanley Miller melaporkan produksi biomolekul dari bahan awal gas sederhana, menggunakan alat yang dibangun untuk mensimulasikan sistem atmosfer-laut Bumi purba. Miller memasukkan 200 ml air, 100 mmHg H₂ , 200 mmHg CH₄ , dan 200 mmHg NH₃ ke dalam alat tersebut, kemudian memaparkan campuran ini, di bawah refluks, pada lucutan listrik selama seminggu, sementara air dipanaskan secara bersamaan. Tujuan manuskrip ini adalah untuk memberikan kepada pembaca protokol eksperimental umum yang dapat digunakan untuk melakukan eksperimen lucutan percikan tipe Miller-Urey, menggunakan labu reaksi 3 L yang disederhanakan. Karena eksperimen ini melibatkan paparan gas yang mudah terbakar terhadap lucutan listrik tegangan tinggi, penting untuk menyoroti langkah-langkah penting yang mengurangi risiko ledakan. Prosedur umum yang dijelaskan dalam karya ini dapat diekstrapolasi untuk merancang dan melakukan berbagai macam eksperimen lucutan listrik yang mensimulasikan lingkungan planet primitif.
Kata kunci: Kimia, Edisi 83, Ilmu Bumi (Umum), Eksobiologi, Miller-Urey, Kimia prabiotik, asam amino, pelepasan percikan api
Perkenalan
Sifat asal usul kehidupan di Bumi tetap menjadi salah satu pertanyaan ilmiah yang paling sulit dipahami. Pada tahun 1920-an, ahli biologi Rusia Alexander Oparin dan ahli biologi evolusi dan genetika Inggris John Haldane mengusulkan konsep "sup primordial" 1,2 , yang menggambarkan lautan terestrial primitif yang mengandung senyawa organik yang mungkin telah memfasilitasi evolusi kimia. Namun, baru pada tahun 1950-an para ahli kimia mulai melakukan studi laboratorium yang disengaja untuk memahami bagaimana molekul organik dapat disintesis dari bahan awal yang sederhana di Bumi purba. Salah satu laporan pertama untuk tujuan ini adalah sintesis asam format dari iradiasi larutan CO2 berair pada tahun 1951 3 .
Pada tahun 1952, Stanley Miller, yang saat itu merupakan mahasiswa pascasarjana di Universitas Chicago, menghubungi Harold Urey untuk melakukan eksperimen guna mengevaluasi kemungkinan bahwa senyawa organik yang penting untuk asal usul kehidupan mungkin telah terbentuk secara abiotik di Bumi purba. Eksperimen tersebut dilakukan menggunakan alat kaca buatan khusus ( Gambar 1A ) yang dirancang untuk mensimulasikan Bumi purba. Eksperimen Miller meniru petir dengan aksi pelepasan listrik pada campuran gas yang mewakili atmosfer purba, dengan adanya reservoir air cair, yang mewakili lautan purba. Alat tersebut juga mensimulasikan penguapan dan presipitasi melalui penggunaan mantel pemanas dan kondensor. Detail spesifik tentang alat yang digunakan Miller dapat ditemukan di tempat lain⁴ . Setelah seminggu terjadi percikan api, isi dalam labu tampak berubah. Air berubah menjadi warna keruh kemerahan⁵ dan material kuning-coklat menumpuk pada elektroda⁴ . Karya inovatif ini dianggap sebagai sintesis biomolekul yang disengaja dan efisien pertama di bawah kondisi Bumi purba yang disimulasikan.
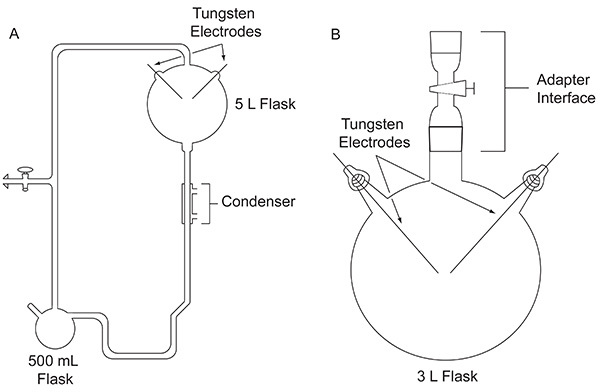 Gambar 1. Perbandingan antara dua jenis peralatan yang dibahas dalam makalah ini. Peralatan klasik yang digunakan untuk percobaan Miller-Urey asli ( A ) dan peralatan sederhana yang digunakan dalam protokol yang diuraikan di sini ( B ). Klik di sini untuk melihat gambar yang lebih besar .
Gambar 1. Perbandingan antara dua jenis peralatan yang dibahas dalam makalah ini. Peralatan klasik yang digunakan untuk percobaan Miller-Urey asli ( A ) dan peralatan sederhana yang digunakan dalam protokol yang diuraikan di sini ( B ). Klik di sini untuk melihat gambar yang lebih besar .
Setelah publikasi hasil eksperimen klasik Miller pada tahun 1953, berbagai variasi eksperimen lucutan percikan, misalnya menggunakan campuran gas lain, dilakukan untuk mengeksplorasi kemungkinan produksi senyawa organik yang penting untuk kehidupan dalam berbagai kondisi awal Bumi. Misalnya, campuran gas CH₄ / H₂O / NH₃ / H₂S diuji kemampuannya untuk menghasilkan asam α-amino yang mengandung sulfur, meskipun senyawa ini tidak terdeteksi⁶ . Analisis kromatografi gas-spektrometri massa (GC-MS) dari campuran CH₄ / NH₃ yang dikenai lucutan listrik menunjukkan sintesis α-aminonitril, yang merupakan prekursor asam amino⁷ . Pada tahun 1972, menggunakan peralatan yang lebih sederhana, yang pertama kali diperkenalkan oleh Oró 8 ( Gambar 1B ), Miller dan rekan-rekannya mendemonstrasikan sintesis semua asam α-amino berkode 9 dan asam amino nonprotein 10 yang telah diidentifikasi dalam meteorit Murchison hingga saat ini, dengan memberikan lucutan listrik pada CH 4 , N 2 , dan sejumlah kecil NH 3. Kemudian, menggunakan desain eksperimental sederhana yang sama, campuran gas yang mengandung H 2 O, N 2 , dan CH 4 , CO 2 , atau CO disuluhkan untuk mempelajari hasil hidrogen sianida, formaldehida, dan asam amino sebagai fungsi dari keadaan oksidasi spesies karbon atmosfer 11 .
Selain eksplorasi desain eksperimental alternatif selama bertahun-tahun, kemajuan analitis yang signifikan telah terjadi sejak eksperimen klasik Miller, yang baru-baru ini membantu investigasi yang lebih mendalam terhadap sampel eksperimental lucutan listrik yang diarsipkan oleh Miller, daripada yang dapat difasilitasi oleh teknik yang dimiliki Miller pada tahun 1950-an. Eksperimen vulkanik Miller¹² , yang pertama kali dilaporkan pada tahun 1955⁴ , dan eksperimen yang mengandung H₂S pada tahun 1958¹³ terbukti telah membentuk variasi yang lebih luas, dan kelimpahan yang lebih besar, dari berbagai asam amino dan amina daripada eksperimen klasik, termasuk banyak di antaranya yang belum pernah diidentifikasi sebelumnya dalam eksperimen lucutan percikan.
Eksperimen yang dijelaskan dalam makalah ini dapat dilakukan menggunakan berbagai campuran gas. Biasanya, setidaknya, eksperimen semacam itu akan mengandung gas yang mengandung C, gas yang mengandung N, dan air. Dengan perencanaan yang matang, hampir semua campuran gas dapat dieksplorasi, namun, penting untuk mempertimbangkan beberapa aspek kimia dari sistem tersebut. Misalnya, pH fase air dapat memiliki dampak signifikan pada kimia yang terjadi di sana 14 .
Metode yang dijelaskan di sini telah disesuaikan untuk menginstruksikan para peneliti cara melakukan eksperimen pelepasan percikan api yang menyerupai eksperimen Miller-Urey menggunakan wadah reaksi 3 L yang disederhanakan, seperti yang dijelaskan dalam publikasi Miller tahun 1972 9,10 . Karena eksperimen ini melibatkan busur listrik tegangan tinggi yang bekerja pada gas yang mudah terbakar, sangat penting untuk menghilangkan O2 dari labu reaksi untuk menghilangkan risiko ledakan, yang dapat terjadi pada pembakaran gas yang mengandung karbon tereduksi seperti metana atau karbon monoksida, atau reaksi H2 dengan oksigen.
Ada beberapa detail tambahan yang perlu diingat saat mempersiapkan pelaksanaan percobaan yang dibahas di sini. Pertama, setiap kali bekerja dengan saluran vakum kaca dan gas bertekanan, terdapat bahaya inheren berupa implosi dan tekanan berlebih. Oleh karena itu, kacamata pengaman harus selalu dikenakan. Kedua, percobaan biasanya dilakukan pada tekanan kurang dari tekanan atmosfer. Ini meminimalkan risiko tekanan berlebih pada manifold dan labu reaksi. Peralatan gelas mungkin diberi peringkat pada atau di atas tekanan atmosfer, namun, tekanan di atas 1 atm tidak disarankan. Tekanan dapat meningkat dalam percobaan ini karena H₂ yang tidak larut dalam air dilepaskan dari gas tereduksi (seperti CH₄ dan NH₃ ) . Tekanan berlebih dapat menyebabkan kebocoran segel, yang dapat memungkinkan O₂ atmosfer masuk ke dalam labu reaksi, sehingga memungkinkan terjadinya pembakaran, yang mengakibatkan ledakan. Ketiga, perlu diingat bahwa modifikasi protokol ini untuk melakukan variasi percobaan memerlukan perencanaan yang cermat untuk memastikan kondisi yang tidak aman tidak tercipta. Keempat, sangat disarankan agar calon peneliti membaca seluruh protokol dengan saksama beberapa kali sebelum mencoba eksperimen ini untuk memastikan bahwa ia memahami potensi kendala dan bahwa semua perangkat keras yang diperlukan tersedia dan terpasang. Terakhir, melakukan eksperimen yang melibatkan gas yang mudah terbakar memerlukan kepatuhan terhadap pedoman Departemen Kesehatan dan Keselamatan Lingkungan lembaga tempat peneliti berafiliasi. Harap perhatikan rekomendasi ini sebelum melanjutkan eksperimen apa pun. Semua langkah yang dirinci dalam protokol di sini sesuai dengan pedoman Kesehatan dan Keselamatan Lingkungan lembaga tempat penulis berafiliasi.
Protokol
1. Memasang Sistem Manifold/Vakum
- Gunakan manifold kaca untuk memasukkan gas ke dalam labu reaksi. Manifold ini dapat dibeli atau dibuat oleh fasilitas pembuatan kaca, tetapi harus mencakup port kedap vakum yang dapat dihubungkan ke sistem vakum, tabung gas, pengukur vakum, dan bejana reaksi.
- Gunakan sambungan kaca gerinda dan sumbat kaca dengan katup pada manifold. Pastikan semua cincin-O pada sumbat mampu membuat segel yang diperlukan. Jika menggunakan sambungan kaca, sejumlah gemuk vakum yang cukup dapat diaplikasikan untuk membantu membuat segel, jika perlu. Gemuk vakum silikon dapat digunakan untuk menghindari potensi kontaminasi organik.
- Gunakan keran kaca pada manifold. Oleskan jumlah minimum gemuk vakum yang diperlukan untuk membuat segel.
- Ukur volume manifold. Volume ini akan digunakan untuk perhitungan yang berkaitan dengan tekanan gas akhir dalam labu reaksi 3 L dan harus diketahui seakurat mungkin.
- Kecuali jika manifold memiliki cukup sambungan untuk menampung semua tabung gas secara bersamaan, sambungkan satu tabung gas ke manifold pada satu waktu. Sertakan pada sambungan ini, sebuah keran yang memungkinkan manifold diisolasi dari atmosfer sekitar.
- Gunakan selang yang sesuai, bersih, inert, dan tahan terhadap bahan kimia serta kebocoran, dan fitting vakum ultratorr untuk menghubungkan tabung gas ke manifold. Fitting ultratorr, jika digunakan, harus dikencangkan dengan tangan.
- Hubungkan ke manifold, pompa vakum yang mampu menghasilkan vakum <1 mmHg. Saluran pembuangan pompa vakum harus ditempatkan di dalam lemari asam, atau dibuang dengan benar melalui cara lain.
- Untuk memastikan tercapainya vakum dengan cepat dan untuk melindungi pompa, pasang perangkap di antara manifold dan pompa vakum. Perangkap jari nitrogen cair direkomendasikan karena akan mencegah zat volatil seperti NH₃ , CO₂ , dan H₂O masuk ke dalam pompa. Perlu berhati-hati, karena zat volatil yang terperangkap, saat memanas, dapat menyebabkan tekanan berlebih pada manifold dan mengakibatkan pecahnya kaca.
- Hubungkan ke manifold, manometer atau alat pengukur vakum lainnya yang mampu mencapai resolusi 1 mmHg atau lebih baik. Meskipun berbagai perangkat dapat digunakan, manometer merkuri, atau pengukur MacLeod, lebih disukai karena merkuri relatif tidak reaktif.
- Ukur dan catat suhu lingkungan menggunakan termometer yang sesuai.
2. Persiapan Labu Reaksi
- Panaskan semua peralatan gelas pada suhu 500 °C selama minimal 3 jam di udara sebelum digunakan, untuk menghilangkan kontaminan organik.
- Bersihkan elektroda tungsten dengan cara mencuci perlahan menggunakan tisu laboratorium bersih dan metanol, lalu keringkan di udara.
- Tuangkan 200 ml air ultra murni (18,2 MΩ cm, <5 ppb TOC) ke dalam labu reaksi 3 L.
- Gunakan batang pengaduk magnetik yang telah dibersihkan dan disterilkan sebelumnya, yang akan memastikan pelarutan cepat gas terlarut dan pencampuran reaktan selama percobaan.
Pasang elektroda tungsten ke labu reaksi 3 L menggunakan sedikit gemuk vakum, dengan ujung-ujung elektroda terpisah sekitar 1 cm di dalam labu. Kencangkan dengan penjepit.
Masukkan adaptor dengan keran terintegrasi ke leher labu reaksi 3 L dan kencangkan dengan penjepit.
- Hubungkan labu reaksi 3 L ke manifold gas melalui adaptor. Gunakan klip atau penjepit untuk membantu mengamankan labu.
- Lumasi semua sambungan dengan sedikit gemuk untuk memastikan penyegelan vakum yang baik.
Buka semua katup dan keran pada manifold, kecuali Katup 6 dan Keran 1 ( Gambar 4 ), dan hidupkan pompa vakum untuk mengosongkan manifold. Setelah pembacaan vakum stabil <1 mmHg tercapai, tutup Katup 1 dan biarkan manifold diam selama ~15 menit untuk memeriksa kebocoran vakum. Jika tidak ada kebocoran yang terdeteksi, lanjutkan ke langkah 2.8. Jika ada kebocoran, periksa berbagai sambungan hingga kebocoran dapat diidentifikasi dan diperbaiki.
Lakukan pengadukan magnetik pada bejana reaksi. Buka Katup 1 dan Keran 1 ( Gambar 4 ) untuk mengosongkan ruang kepala labu reaksi 3 L hingga tekanannya mencapai <1 mmHg.
Tutup Katup 1 ( Gambar 4 ) dan pantau tekanan di dalam labu reaksi 3 L. Tekanan yang terukur seharusnya meningkat hingga tekanan uap air. Untuk memastikan tidak ada kebocoran, tunggu sekitar 5 menit pada tahap ini. Jika tekanan (seperti yang terbaca pada manometer) meningkat saat Katup 1 tertutup selama langkah ini, periksa kebocoran pada Keran 1 dan berbagai sambungan labu reaksi. Jika tidak ditemukan kebocoran, lanjutkan ke langkah berikutnya.
3. Pengenalan Gas NH3
Hitung tekanan gas NH₃ yang diperlukan untuk dimasukkan ke dalam manifold sehingga 200 mmHg NH₃ akan masuk ke dalam labu reaksi. Detail tentang cara melakukannya diberikan di bagian Diskusi.
Tutup Katup 1 dan 6, serta Keran Penghenti 1 ( Gambar 4 ) sebelum memasukkan gas apa pun ke dalam manifold. Biarkan katup dan keran penghenti lainnya tetap terbuka.
Masukkan NH3 ke dalam manifold hingga tekanan rendah (sekitar 10 mmHg) tercapai, lalu kosongkan manifold hingga tekanan <1 mmHg dengan membuka Katup 1 ( Gambar 4 ). Ulangi 3 kali.
Masukkan NH3 ke dalam manifold untuk mencapai tekanan yang ditentukan pada langkah 3.1.
Buka keran 1 ( Gambar 4 ) untuk memasukkan NH₃ dengan tekanan 200 mmHg ke dalam labu reaksi 3 L. NH₃ akan larut dalam air di dalam labu reaksi dan tekanan akan turun perlahan.
Setelah tekanan berhenti turun, tutup Stopcock 1 ( Gambar 4 ) dan catat tekanan yang terbaca oleh manometer. Nilai ini mewakili tekanan di dalam labu dan akan digunakan untuk menghitung tekanan gas lain yang akan dimasukkan ke dalam manifold nanti.
Buka Katup 1 ( Gambar 4 ) untuk mengosongkan manifold hingga tekanan <1 mmHg.
Tutup Katup 2 ( Gambar 4 ) dan lepaskan tabung gas NH3 dari manifold.
4. Pengenalan Bab 4
Hitung tekanan CH₄ yang diperlukan untuk dimasukkan ke dalam manifold sehingga 200 mmHg CH₄ akan masuk ke dalam labu reaksi 3 L. Contoh perhitungan ditunjukkan pada bagian Diskusi.
Hubungkan tabung gas CH4 ke manifold.
Buka semua katup dan keran, kecuali Katup 6 dan Keran 1 ( Gambar 4 ), dan kosongkan manifold hingga tekanan <1 mmHg.
Tutup Katup 1 setelah manifold dikosongkan ( Gambar 4 ).
Masukkan CH4 ke dalam manifold hingga diperoleh tekanan kecil (sekitar 10 mmHg). Ini membersihkan saluran dari gas-gas kontaminan dari langkah-langkah sebelumnya. Buka Katup 1 ( Gambar 4 ) untuk mengosongkan manifold hingga <1 mmHg. Ulangi 2x lagi.
Masukkan CH4 ke dalam manifold hingga tekanan yang dihitung pada langkah 4.1 tercapai.
Buka keran 1 ( Gambar 4 ) untuk memasukkan 200 mmHg CH4 ke dalam labu reaksi 3 L.
Tutup keran 1 setelah tekanan CH4 yang diinginkan dimasukkan ke dalam labu reaksi 3 L ( Gambar 4 ) dan catat tekanan yang diukur oleh manometer.
Buka Katup 1 (Gambar 4 ) untuk mengosongkan manifold hingga <1 mmHg.
Tutup Katup 2 ( Gambar 4 ) dan lepaskan silinder CH 4 dari manifold.
5. Pengenalan Gas Tambahan ( misalnya N2 )
Pada tahap ini, tidak perlu menambahkan gas tambahan. Namun, jika diinginkan, disarankan untuk menambahkan 100 mmHg N₂ . Dalam hal ini, hitung tekanan N₂ yang diperlukan untuk dimasukkan ke dalam manifold sehingga 100 mmHg N₂ akan masuk ke dalam labu reaksi 3 L. Contoh perhitungan ditunjukkan pada bagian Diskusi.
Hubungkan tabung gas N2 ke manifold.
Buka semua katup dan keran, kecuali Katup 6 dan Keran 1 ( Gambar 4 ), dan kosongkan manifold hingga tekanan <1 mmHg.
Tutup Katup 1 setelah manifold dikosongkan ( Gambar 4 ).
Masukkan N2 ke dalam manifold hingga diperoleh tekanan kecil (sekitar 10 mmHg). Buka Katup 1 ( Gambar 4 ) untuk mengosongkan manifold hingga <1 mmHg. Ulangi 2x lagi.
Masukkan N2 ke dalam manifold hingga tekanan yang dihitung pada langkah 5.1 tercapai.
Buka keran 1 ( Gambar 4 ) untuk memasukkan 100 mmHg N2 ke dalam labu reaksi.
Tutup keran 1 setelah tekanan N2 yang diinginkan dimasukkan ke dalam labu reaksi ( Gambar 4 ), dan catat tekanannya menggunakan manometer.
Buka Katup 1 ( Gambar 4 ) untuk mengosongkan manifold hingga <1 mmHg.
Tutup Katup 2 ( Gambar 4 ) dan lepaskan silinder N2 dari manifold.
6. Memulai Percobaan
Lepaskan labu reaksi dari manifold dengan menutup Stopcock 1 dan Valve 1 ( Gambar 4 ) setelah semua gas dimasukkan ke dalam labu reaksi, sehingga udara sekitar dapat masuk ke manifold dan menaikkan tekanan manifold hingga mencapai tekanan sekitar.
Setelah melepaskan labu reaksi dari manifold dengan hati-hati, letakkan labu di tempat yang tidak akan terganggu ( misalnya di dalam lemari asam yang kosong).
Lepaskan pompa vakum dan lepaskan perangkap dingin dengan hati-hati, lalu biarkan udara keluar ke dalam lemari asap yang berfungsi penuh.
Amankan kumparan Tesla yang terhubung ke generator percikan frekuensi tinggi.
Hubungkan elektroda tungsten yang berlawanan ke ground listrik untuk memungkinkan arus listrik mengalir secara efisien melalui celah antara kedua elektroda.
Atur tegangan keluaran generator percikan api ke sekitar 30.000 V, seperti yang dijelaskan dalam dokumen yang tersedia dari pabrikan.
Sebelum memulai percikan api, tutup penutup lemari asam, untuk berfungsi sebagai pelindung keselamatan antara peralatan dan peneliti. Hidupkan kumparan Tesla untuk memulai percobaan, dan biarkan percikan api berlanjut selama 2 minggu (atau periode lain yang diinginkan) dalam siklus hidup/mati 1 jam.
7. Akhir Percobaan
Hentikan percobaan dengan mematikan kumparan Tesla.
Buka keran 1 ( Gambar 4 ) untuk memasukkan udara sekitar secara perlahan ke dalam labu reaksi dan memudahkan pelepasan adaptor dan elektroda tungsten sehingga sampel dapat dikumpulkan. Jika diinginkan, vakum dapat digunakan untuk mengeluarkan gas reaksi berbahaya dari labu reaksi.
8. Mengambil Sampel Cairan
- Dengan menggunakan pipet kaca yang telah dipirolisis, ambil sampel cairan dari labu reaksi, berhati-hatilah untuk meminimalkan paparan terhadap kontaminan, seperti yang mungkin masuk akibat pipet menyentuh gemuk vakum atau permukaan nonsteril lainnya.
- Pindahkan sampel ke wadah plastik atau kaca steril. Wadah plastik lebih tahan terhadap retak atau pecah saat dibekukan, dibandingkan dengan wadah kaca.
Tutup rapat wadah sampel dan simpan di dalam freezer yang mampu mencapai suhu -20 °C atau lebih rendah, karena produk yang tidak larut dapat mencegah larutan sampel membeku pada suhu 0 °C.
9. Membersihkan Peralatan
Gunakan tisu laboratorium bersih untuk membersihkan gemuk vakum dengan hati-hati dari leher alat, adaptor dan keran, serta kaca yang mengelilingi elektroda tungsten.
Bersihkan secara menyeluruh permukaan yang sama seperti yang dijelaskan pada langkah 9.1 dengan toluena untuk menghilangkan sepenuhnya gemuk vakum organik dari peralatan gelas. Jika menggunakan gemuk silikon, gemuk vakum tinggi mungkin tetap menempel pada peralatan gelas setelah pirolisis, yang dapat menimbulkan masalah di kemudian hari, seperti yang dijelaskan secara rinci di bagian Diskusi.
Bersihkan labu reaksi secara menyeluruh dengan sikat dan pelarut berikut secara berurutan: air ultra murni (18,2 MΩ cm, <5 ppb TOC), air ultra murni (18,2 MΩ cm, <5 ppb TOC) dengan 5% deterjen pembersih, metanol, toluena, metanol, air ultra murni (18,2 MΩ cm, <5 ppb TOC) dengan 5% deterjen pembersih, dan terakhir air ultra murni (18,2 MΩ cm, <5 ppb TOC).
Tutup semua lubang terbuka pada labu reaksi dengan kertas aluminium dan bungkus adaptor beserta komponen-komponennya dengan kertas aluminium.
Setelah semua peralatan gelas dibungkus dengan aluminium foil, lakukan pirolisis selama minimal 3 jam di udara pada suhu 500 °C.
Bersihkan elektroda dengan lembut menggunakan metanol dan biarkan mengering di udara.
10. Analisis Sampel
Catatan: Saat menyiapkan sampel untuk analisis, penggunaan protokol hidrolisis asam seperti yang telah dijelaskan secara rinci di tempat lain 15 , berguna untuk mendapatkan lebih banyak asam amino. Hidrolisis sebagian sampel yang diperoleh memberikan kesempatan untuk menganalisis baik asam amino bebas maupun prekursornya yang labil terhadap asam yang disintesis dalam kondisi abiotik.
Untuk analisis asam amino, gunakan teknik yang sesuai (seperti kromatografi cair dan metode berbasis spektrometri massa, atau pendekatan lain yang tepat). Teknik analitik tersebut meliputi kromatografi cair kinerja tinggi dengan deteksi fluoresensi (HPLC-FD) 14 , dan kromatografi cair kinerja ultra tinggi dengan deteksi fluoresensi secara paralel dengan spektrometri massa ionisasi elektrospray positif waktu terbang (UHPLC-FD/ToF-MS) 12,13 . Manuskrip ini menjelaskan analisis menggunakan analisis spektrometri massa melalui spektrometer massa kuadrupol rangkap tiga (QqQ-MS) bersamaan dengan HPLC-FD.
Hasil Representatif
Produk yang disintesis dalam eksperimen lucutan listrik dapat cukup kompleks, dan terdapat banyak pendekatan analitis yang dapat digunakan untuk mempelajarinya. Beberapa teknik yang lebih umum digunakan dalam literatur untuk menganalisis asam amino dibahas di sini. Metode kromatografi dan spektrometri massa merupakan teknik yang sangat informatif untuk menganalisis campuran kimia kompleks yang dihasilkan oleh eksperimen lucutan percikan tipe Miller-Urey. Analisis asam amino dapat dilakukan menggunakan o- ftaldialdehida/N-asetil-L-sistein (OPA/NAC) 16 , pasangan reagen kiral yang menandai gugus amino primer, menghasilkan turunan diastereomer fluoresen yang dapat dipisahkan pada fase stasioner akiral. Gambar 2 menunjukkan kromatogram standar asam amino yang didervatisasi OPA/NAC yang diperoleh dengan HPLC yang digabungkan dengan deteksi fluoresensi dan QqQ-MS. Asam amino yang terkandung dalam standar tersebut termasuk yang biasanya dihasilkan dalam eksperimen lucutan percikan tipe Miller-Urey. Identitas asam amino ini tercantum dalam Tabel 1 . Jejak fluoresensi representatif dari sampel tipikal dan blanko analitik ditunjukkan pada Gambar 3 , yang menunjukkan kompleksitas molekuler sampel lucutan listrik tipe Miller-Urey. Kromatogram sampel pada Gambar 3 dihasilkan dari percobaan lucutan percikan menggunakan kondisi awal berikut: 300 mmHg CH₄ , 250 mmHg NH₃ , dan 250 ml air.
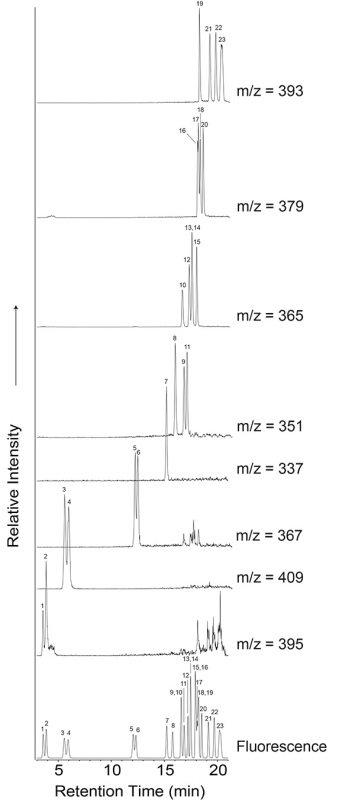 Gambar 2. Wilayah 3-21 menit dari kromatogram HPLC-FD/QqQ-MS yang dihasilkan dari analisis standar asam amino yang didervatisasi OPA/NAC . Identitas puncak asam amino tercantum dalam Tabel 1. Jejak fluoresensi ditunjukkan di bagian bawah dan kromatogram massa terekstraksi yang sesuai ditunjukkan di atas. Ionisasi elektrospray (ESI) QqQ-MS dioperasikan dalam mode positif dan memantau rentang massa 50-500 m/z. Pengaturan ESI adalah: suhu gas desolvasi (N2 ) : 350 °C, 650 L/jam; tegangan kapiler: 3,8 kV; tegangan kerucut: 30 V. Puncak yang tidak berlabel dalam kromatogram ion terekstraksi 367 adalah puncak 13C2 dari kromatogram ion terekstraksi 365, sebagai hasil dari kelimpahan alami 13C sekitar 1%. Klik di sini untuk melihat gambar yang lebih besar .
Gambar 2. Wilayah 3-21 menit dari kromatogram HPLC-FD/QqQ-MS yang dihasilkan dari analisis standar asam amino yang didervatisasi OPA/NAC . Identitas puncak asam amino tercantum dalam Tabel 1. Jejak fluoresensi ditunjukkan di bagian bawah dan kromatogram massa terekstraksi yang sesuai ditunjukkan di atas. Ionisasi elektrospray (ESI) QqQ-MS dioperasikan dalam mode positif dan memantau rentang massa 50-500 m/z. Pengaturan ESI adalah: suhu gas desolvasi (N2 ) : 350 °C, 650 L/jam; tegangan kapiler: 3,8 kV; tegangan kerucut: 30 V. Puncak yang tidak berlabel dalam kromatogram ion terekstraksi 367 adalah puncak 13C2 dari kromatogram ion terekstraksi 365, sebagai hasil dari kelimpahan alami 13C sekitar 1%. Klik di sini untuk melihat gambar yang lebih besar .
Tabel 1. Identitas puncak untuk asam amino yang terdeteksi dalam standar dan yang biasanya dihasilkan dalam eksperimen lucutan percikan tipe Miller-Urey.
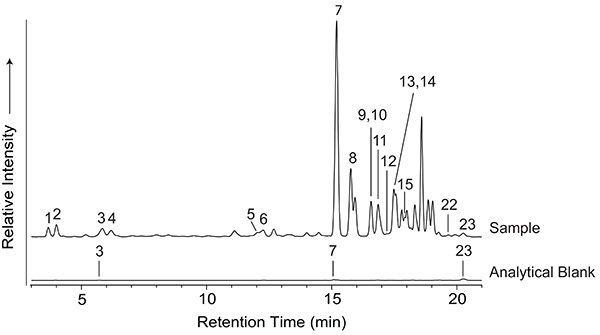 Gambar 3. Wilayah 3-21 menit dari kromatogram HPLC-FD yang mewakili eksperimen pelepasan percikan tipe Miller-Urey. Puncak-puncak diidentifikasi dan dikuantifikasi berdasarkan waktu retensi dan analisis massa senyawa target dibandingkan dengan standar dan blanko analitik. Semua analit target dengan waktu retensi fluoresensi yang berelusi bersama dapat dipisahkan dan dikuantifikasi menggunakan spektrometri massa, kecuali α-AIB dan L-β-ABA (puncak 13 dan 14), dan D/L-norleusin, yang berelusi bersama dengan D/L-leusin (puncak 23), di bawah kondisi kromatografi yang digunakan. D/L-norleusin ditambahkan sebagai standar internal ke sampel dan blanko analitik selama persiapan sampel. Pemisahan asam amino dicapai menggunakan kolom HPLC Phenyl-Hexyl berukuran 4,6 mm x 250 mm, dengan ukuran partikel 5 μm. Fase gerak terdiri dari: A) air ultra murni (18,2 MΩ cm, <5 ppb TOC), B) metanol, dan C) 50 mM amonium format dengan 8% metanol, pada pH 8. Gradien yang digunakan adalah: 0-5 menit, 100% C; 5-15 menit, 0-83% A, 0-12% B, 100-5% C; 15-22 menit, 83-75% A, 12-20% B, 5% C; 22-35 menit, 75-35% A, 20-60% B, 5% C; 35-37 menit, 35-0% A, 60-100% B, 5-0% C; 37-45 menit, 100% B; 45-46 menit, 100-0% B, 0-100% C. 46-55 menit, 100% C. Laju alir adalah 1 ml/menit. Klik di sini untuk melihat gambar yang lebih besar .
Gambar 3. Wilayah 3-21 menit dari kromatogram HPLC-FD yang mewakili eksperimen pelepasan percikan tipe Miller-Urey. Puncak-puncak diidentifikasi dan dikuantifikasi berdasarkan waktu retensi dan analisis massa senyawa target dibandingkan dengan standar dan blanko analitik. Semua analit target dengan waktu retensi fluoresensi yang berelusi bersama dapat dipisahkan dan dikuantifikasi menggunakan spektrometri massa, kecuali α-AIB dan L-β-ABA (puncak 13 dan 14), dan D/L-norleusin, yang berelusi bersama dengan D/L-leusin (puncak 23), di bawah kondisi kromatografi yang digunakan. D/L-norleusin ditambahkan sebagai standar internal ke sampel dan blanko analitik selama persiapan sampel. Pemisahan asam amino dicapai menggunakan kolom HPLC Phenyl-Hexyl berukuran 4,6 mm x 250 mm, dengan ukuran partikel 5 μm. Fase gerak terdiri dari: A) air ultra murni (18,2 MΩ cm, <5 ppb TOC), B) metanol, dan C) 50 mM amonium format dengan 8% metanol, pada pH 8. Gradien yang digunakan adalah: 0-5 menit, 100% C; 5-15 menit, 0-83% A, 0-12% B, 100-5% C; 15-22 menit, 83-75% A, 12-20% B, 5% C; 22-35 menit, 75-35% A, 20-60% B, 5% C; 35-37 menit, 35-0% A, 60-100% B, 5-0% C; 37-45 menit, 100% B; 45-46 menit, 100-0% B, 0-100% C. 46-55 menit, 100% C. Laju alir adalah 1 ml/menit. Klik di sini untuk melihat gambar yang lebih besar .
Diskusi
Sejumlah langkah dalam protokol yang dijelaskan di sini sangat penting untuk melakukan eksperimen tipe Miller-Urey dengan aman dan benar. Pertama, semua peralatan gelas dan alat penanganan sampel yang akan bersentuhan dengan labu reaksi atau sampel perlu disterilkan. Sterilisasi dilakukan dengan membilas peralatan tersebut secara menyeluruh dengan air ultra murni (18,2 MΩ cm, <5 ppb TOC) dan kemudian membungkusnya dengan aluminium foil, sebelum dipirolisis pada suhu 500 °C di udara selama minimal 3 jam. Setelah peralatan dipirolisis dan saat menyiapkan sampel untuk analisis, harus berhati-hati untuk menghindari kontaminasi organik. Risiko kontaminasi dapat diminimalkan dengan mengenakan sarung tangan nitril, jas laboratorium, dan kacamata pelindung. Pastikan untuk bekerja dengan sampel jauh dari tubuh karena sumber kontaminasi umum meliputi sidik jari, kulit, rambut, dan napas yang dihembuskan. Hindari kontak dengan sarung tangan basah dan jangan gunakan bahan lateks atau nilon. Kedua, penghilangan gas secara menyeluruh dari labu reaksi sebelum penambahan gas ke dalam labu reaksi sangat penting. Keberadaan oksigen molekuler dalam jumlah kecil sekalipun di dalam labu reaksi menimbulkan risiko ledakan ketika percikan api dilepaskan ke dalam gas yang mudah terbakar seperti CH₄ . Saat proses penghilangan gas dari labu, air di dalam labu akan mendidih, yang akan mencegah pembacaan yang stabil. Pada tahap ini ada dua pilihan: 1) menghilangkan gas dari labu melalui siklus pembekuan-pencairan (biasanya 3 kali digunakan), atau 2) cukup menghilangkan gas dari larutan cair. Dalam kasus terakhir, sebagian air akan hilang, namun jumlahnya relatif kecil dibandingkan dengan volume yang tersisa. Ketiga, pengaturan yang lengkap dan efisien harus dibangun dengan cermat untuk menghasilkan percikan api yang konsisten di seluruh elektroda selama keseluruhan percobaan. Kumparan Tesla BD-50E tidak dirancang untuk pengoperasian yang lama, karena ditujukan untuk deteksi kebocoran vakum. Oleh karena itu, pendinginan berkala pada kumparan Tesla direkomendasikan untuk memperpanjang masa pakai operasional. Ada beberapa cara untuk mencapai hal ini. Salah satu cara sederhana adalah dengan memasang timer secara seri antara penguji percikan api dan catu dayanya, lalu memprogram timer tersebut agar bergantian dalam siklus hidup/mati 1 jam. Pendinginan kumparan Tesla dengan kipas komersial mungkin juga diperlukan untuk memperpanjang umur kumparan Tesla. Ujung kumparan Tesla harus menyentuh atau hampir menyentuh salah satu elektroda tungsten; jarak antara keduanya sekitar 1 mm atau kurang. Selain itu, pelepasan muatan yang intens dapat dicapai dengan menggunakan kawat logam konduktif dengan lingkaran di salah satu ujungnya yang dililitkan dengan ringan di atas elektroda yang berlawanan dengan elektroda yang menyentuh kumparan Tesla untuk menghindari rusaknya segel ke isinya. Disarankan juga untuk memiliki generator percikan api kedua jika generator percikan api utama gagal karena penggunaan yang lama.
Ada banyak catatan tambahan yang perlu diingat saat melakukan berbagai langkah dalam protokol yang diuraikan di sini. Saat menyiapkan sistem manifold untuk suatu percobaan dan menggunakan manometer merkuri, umumnya disepakati bahwa presisi 1 mmHg adalah yang terbaik yang dapat dicapai, karena resolusi mata manusia. Beberapa gas mungkin menimbulkan masalah konduktivitas dengan pengukur berbasis resistansi. Manometer merkuri berpotensi menimbulkan bahaya tumpahan, yang harus dipersiapkan sebelumnya.
Saat merakit labu reaksi 3 L, penggunaan gemuk vakum silikon dapat mengurangi potensi kontaminasi organik, tetapi perlu diperhatikan untuk membersihkannya secara menyeluruh di antara setiap percobaan. Kegagalan untuk melakukannya akan mengakibatkan penumpukan endapan silika selama pirolisis suhu tinggi, yang dapat mengganggu segel vakum. Selain itu, elektroda tungsten tersedia secara komersial sebagai tungsten 2% thoriated dan harus dianil ke dalam fitting kaca setengah lingkaran . Jangan memirolisis elektroda tungsten yang terpasang pada kaca di dalam oven. Koefisien ekspansi termal tungsten dan kaca berbeda dan pemanasan di atas 100 °C dapat melemahkan segel di sekitar elektroda yang dianil pada kaca dan menyebabkan kebocoran pada sistem. Selain itu, air ultra murni dapat dimasukkan ke dalam labu reaksi 3 L dengan cara menuang, dengan hati-hati agar tidak bersentuhan dengan gemuk pada port yang digunakan, atau dengan memipet, menggunakan pipet kaca yang telah dipirolisis sebelumnya. Fase air dalam labu reaksi dapat di-buffer, jika diinginkan. Misalnya, Miller dan rekan-rekannya 9 menyangga larutan hingga pH ~8,7 dengan buffer NH 3 /NH 4 Cl. Untuk melakukan ini, fase air dibuat 0,05 M dalam NH 4 Cl sebelum dimasukkan ke dalam labu reaksi. NH 4 Cl dengan kemurnian 99,5% atau lebih tinggi harus digunakan. Sisa NH 3 kemudian ditambahkan ke dalam labu reaksi sebagai gas.
Sebagai persiapan untuk memasukkan gas ke dalam labu reaksi 3 L, labu dapat diamankan pada manifold dengan menempatkan labu di atas cincin gabus, diletakkan di atas dongkrak laboratorium, dan perlahan-lahan mengangkat rakitan labu hingga terpasang rapat. Saat memeriksa kebocoran, perlu diperhatikan bahwa kemungkinan sumber kebocoran meliputi segel yang buruk pada sambungan sambungan kaca setengah lingkaran, yang menghubungkan elektroda tungsten ke labu reaksi, dan keran adaptor yang terpasang pada leher labu reaksi 3 L. Jika kebocoran dari sumber-sumber ini terdeteksi, lepaskan labu reaksi 3 L dari manifold dengan hati-hati, bersihkan area tersebut dengan tisu laboratorium yang bersih, oleskan kembali lapisan gemuk vakum yang baru, dan pasang kembali labu ke manifold untuk mencari kebocoran. Jika tidak ditemukan kebocoran, lanjutkan memasukkan gas ke dalam labu reaksi.
Saat memasukkan gas ke dalam peralatan, tabung gas harus diikat dengan aman ke penyangga. Perlu diperhatikan untuk memasukkan gas secara perlahan. Katup pada tabung gas harus dibuka perlahan dan hati-hati sambil memantau manometer untuk menghindari tekanan berlebih pada peralatan gelas dan fitting yang terpasang. Penting untuk dicatat bahwa saat menambahkan NH₃ ke dalam labu reaksi, karena NH₃ cukup larut dalam air di bawah pKa NH₄⁺ ( ~9,2 ) , pada dasarnya semua gas NH₃ yang dimasukkan ke dalam manifold akan larut dalam fase air, sehingga tekanan akhir dalam labu dan manifold sama dengan tekanan uap air pada suhu ruangan. Setelah tekanan ini tercapai, dapat diasumsikan bahwa transfer telah selesai. Berikut adalah contoh perhitungan yang harus dilakukan untuk memasukkan gas ke dalam labu reaksi secara tepat pada tekanan yang diinginkan:
Pengenalan Gas NH₃
Karena kelarutan NH₃ , pada dasarnya semua NH₃ akan berpindah dari manifold ke labu reaksi dan larut dalam fase air selama tekanan NH₃ di manifold lebih tinggi daripada tekanan uap air di dalam labu reaksi. Oleh karena itu, suhu lingkungan harus dicatat dan tekanan uap air pada suhu tersebut harus dijadikan acuan sebelum memasukkan NH₃ ke dalam manifold. Tekanan target NH₃ yang akan dimasukkan ke dalam labu reaksi harus sama dengan tekanan target NH₃ di dalam labu reaksi 3 L, ditambah tekanan uap air di dalam labu reaksi, pada suhu lingkungan yang tercatat. Misalnya, pada 25 °C, tekanan uap air sekitar 24 mmHg. Oleh karena itu, untuk memasukkan 200 mmHg NH₃ ke dalam labu reaksi, masukkan sekitar 225 mmHg NH₃ ke dalam manifold sebelum memindahkan NH₃ dari manifold ke dalam labu reaksi. Hal ini akan menghasilkan sekitar 200 mmHg NH₃ yang dimasukkan ke dalam labu reaksi.
Pengenalan Bab 4
Setelah penambahan NH₃ dan pelarutannya dalam fase air, tekanan di ruang kepala labu reaksi akan sama dengan tekanan uap air pada 25 °C, sekitar 24 mmHg. Nilai ini akan digunakan, bersama dengan contoh manifold yang ditunjukkan pada Gambar 4 , untuk melakukan perhitungan berapa banyak CH₄ yang harus dimasukkan ke dalam manifold sehingga 200 mmHg CH₄ akan dimasukkan ke dalam labu reaksi:
P 1 = tekanan total yang diinginkan di seluruh sistem, termasuk labu reaksi V 1 = volume total seluruh sistem, termasuk labu reaksi
P 2 = tekanan CH 4 yang dibutuhkan untuk mengisi volume manifold sebelum dimasukkan ke dalam labu reaksi V 2 = volume manifold yang digunakan untuk pemasukan gas
P 3 = tekanan yang sudah ada di ruang kepala labu reaksi V 3 = volume labu reaksi
P 1 = 200 mmHg CH 4 + 24 mmHg H 2 O = 224 mmHg V 1 = 3.000 ml + 100 ml + 300 ml + 40 ml + 20 ml + 3.000 ml + 40 ml + 500 ml = 7.000 ml
P 2 = tekanan CH 4 yang dihitung V 2 = 100 ml + 300 ml + 40 + 20 + 3.000 ml + 40 ml + 500 ml = 4.000 ml
P 3 = 24 mmHg H 2 O V 3 = 3.000 ml
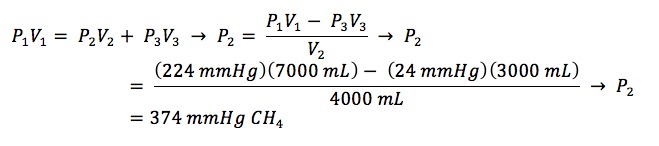
Pengenalan N 2
Setelah dimasukkannya CH₄ , ruang kosong di dalam labu reaksi terisi oleh 200 mmHg CH₄ dan 24 mmHg H₂O, sehingga totalnya menjadi 224 mmHg. Nilai ini akan digunakan, bersama dengan dimensi manifold contoh yang ditunjukkan pada Gambar 4 , untuk menghitung tekanan N₂ yang perlu dimasukkan ke dalam manifold sehingga 100 mmHg N₂ akan masuk ke dalam labu reaksi:
P 1 = tekanan total yang diinginkan di seluruh sistem, termasuk labu reaksi V 1 = volume total seluruh sistem, termasuk labu reaksi
P 2 = tekanan N 2 yang dibutuhkan untuk mengisi volume manifold sebelum dimasukkan ke dalam labu reaksi V 2 = volume manifold yang digunakan untuk pemasukan gas
P 3 = tekanan yang sudah ada di ruang kepala labu reaksi V 3 = volume labu reaksi
P 1 = 24 mmHg H 2 O + 200 mmHg CH 4 + 100 mmHg N 2 = 324 mmHg V 1 = 3.000 ml + 100 ml > + 300 ml + 40 ml + 20 ml + 3.000 ml + 40 ml + 500 ml = 7.000 ml
P 2 = tekanan N 2 yang sedang dihitung V 2 = 100 ml + 300 ml + 40 ml + 20 ml + 3.000 ml + 40 ml + 500 ml = 4.000 ml
P 3 = 200 mmHg CH 4 + 24 mmHg H 2 O = 224 mmHg V 3 = 3.000 ml
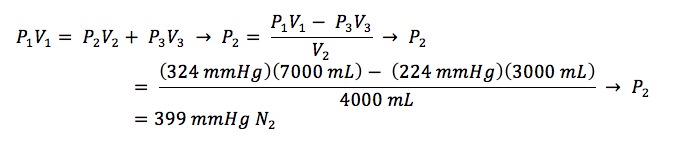
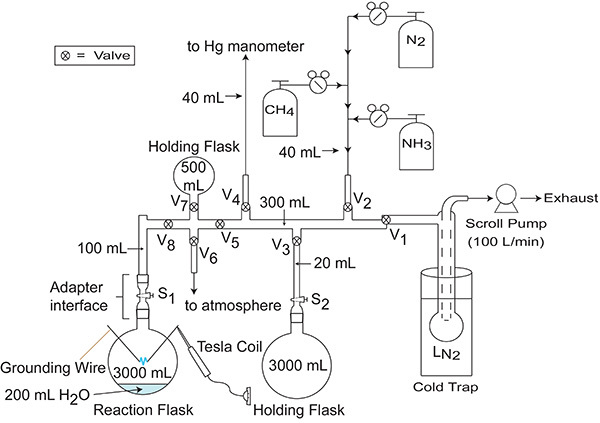 Gambar 4. Sistem manifold/vakum yang digunakan untuk memasukkan gas ke dalam labu reaksi 3 L. Katup yang mengontrol aliran gas diberi label V 1 - V 8 , sedangkan keran pengatur aliran gas diberi label S 1 dan S 2. Perlu dicatat bahwa meskipun Katup 1, 2, dan 6, serta Keran Pengatur Aliran 1 secara eksplisit disebutkan dalam protokol, katup dan keran pengatur aliran lainnya pada manifold yang ditunjukkan di sini berguna untuk menambah atau mengurangi volume ( yaitu labu penampung) ke atau dari manifold. Misalnya, ketika memasukkan gas ke dalam manifold pada tekanan yang relatif tinggi (sekitar 500 mmHg atau lebih), disarankan agar peneliti menggunakan semua labu pembersih yang terpasang pada manifold untuk meningkatkan volume manifold yang dapat diakses dan membantu meminimalkan risiko tekanan berlebih pada manifold.
Gambar 4. Sistem manifold/vakum yang digunakan untuk memasukkan gas ke dalam labu reaksi 3 L. Katup yang mengontrol aliran gas diberi label V 1 - V 8 , sedangkan keran pengatur aliran gas diberi label S 1 dan S 2. Perlu dicatat bahwa meskipun Katup 1, 2, dan 6, serta Keran Pengatur Aliran 1 secara eksplisit disebutkan dalam protokol, katup dan keran pengatur aliran lainnya pada manifold yang ditunjukkan di sini berguna untuk menambah atau mengurangi volume ( yaitu labu penampung) ke atau dari manifold. Misalnya, ketika memasukkan gas ke dalam manifold pada tekanan yang relatif tinggi (sekitar 500 mmHg atau lebih), disarankan agar peneliti menggunakan semua labu pembersih yang terpasang pada manifold untuk meningkatkan volume manifold yang dapat diakses dan membantu meminimalkan risiko tekanan berlebih pada manifold.
Setelah memulai percobaan, sistem harus diperiksa secara berkala untuk memastikan percobaan berjalan dengan benar. Hal-hal yang perlu diperiksa meliputi: 1) generator percikan menghasilkan percikan, dan 2) percikan dihasilkan di antara elektroda tungsten secara terus menerus. Jika kondisi di atas tidak terpenuhi, lepaskan kumparan Tesla dari catu daya dan ganti dengan kumparan Tesla cadangan. Sementara itu, perbaikan pada kumparan Tesla yang rusak dapat dilakukan. Seringkali, pelat kontak di dalam rumah generator percikan dapat mengalami korosi akibat penggunaan yang lama dan harus dipoles, atau diganti.
Setelah percobaan selesai, gas-gas di ruang kepala (head-space) dapat mengiritasi sistem pernapasan. Gas-gas berbahaya, seperti hidrogen sianida 4, dapat dihasilkan oleh percobaan ini. Jika peneliti tidak mengumpulkan sampel gas untuk analisis, ada baiknya menghubungkan alat ke aspirator air untuk mengeluarkan zat volatil selama kurang lebih satu jam setelah percobaan selesai, sementara alat tetap berada di dalam lemari asam (fume hood), sebelum mengumpulkan sampel cairan. Demi alasan keamanan, disarankan agar alat tersebut diangin-anginkan di dalam lemari asam yang berfungsi penuh. Pengumpulan sampel harus dilakukan di dalam lemari asam yang berfungsi dan penanganan sampel di bangku aliran bertekanan positif yang disaring HEPA direkomendasikan.
Di antara berbagai jenis produk yang terbentuk melalui percobaan lucutan percikan, asam amino memiliki arti penting. Asam amino mudah disintesis melalui sintesis Strecker 17. Sintesis asam amino Strecker melibatkan reaksi aldehida atau keton dan HCN yang dihasilkan oleh aksi lucutan listrik pada gas yang dimasukkan ke dalam alat reaksi, yang setelah larut dalam fase air, dapat bereaksi dengan amonia untuk membentuk α-aminonitril yang mengalami hidrolisis untuk menghasilkan asam amino. Ini, tentu saja, hanyalah satu mekanisme sintesis, dan mekanisme lain juga dapat beroperasi, seperti aminasi langsung prekursor termasuk akrilonitril untuk menghasilkan prekursor β-alanin, atau hidrolisis langsung bahan seperti tholin dengan berat molekul lebih tinggi untuk menghasilkan asam amino secara langsung, melewati mekanisme Strecker.
Kontaminasi asam amino pada sampel yang dihasilkan oleh eksperimen Miller-Urey dapat terjadi jika tindakan pencegahan yang disebutkan sebelumnya tidak diikuti secara eksplisit. Selama analisis sampel, penting untuk mencari tanda-tanda kontaminasi terestrial yang mungkin berasal dari penanganan atau penyimpanan sampel. Penggunaan OPA/NAC 16 bersamaan dengan teknik LC-FD memungkinkan pemisahan kromatografi enantiomer D- dan L- dari asam amino dengan pusat kiral dan kuantifikasi masing-masing secara individual. Asam amino kiral yang disintesis oleh eksperimen seharusnya bersifat rasemik. Kesalahan eksperimental yang dapat diterima selama sintesis asam amino dengan pusat kiral umumnya dianggap sekitar 10%. Oleh karena itu, rasio D/L asam amino kiral yang menunjukkan pengayaan salah satu enantiomer lebih dari 10% merupakan metrik yang baik untuk menentukan apakah sampel telah terkontaminasi.
Metode yang disajikan di sini dimaksudkan untuk memberikan petunjuk tentang cara melakukan percobaan pelepasan percikan api tipe Miller-Urey; namun, ada beberapa keterbatasan pada teknik yang dijelaskan di sini yang perlu diperhatikan. Pertama, pemanasan labu reaksi tunggal 3 L ( Gambar 1B ) akan mengakibatkan kondensasi uap air pada ujung elektroda, meredam percikan api, dan mengurangi pembentukan spesies radikal yang mendorong sebagian besar reaksi kimia yang terjadi dalam percobaan. Selanjutnya, penggunaan mantel pemanas untuk memanaskan peralatan tidak diperlukan untuk mensintesis senyawa organik, seperti asam amino. Hal ini berbeda dengan percobaan asli Miller di mana ia menggunakan peralatan labu ganda yang lebih kompleks dan dibuat khusus ( Gambar 1A ) 5 dan memanaskan labu kecil di bagian bawah peralatan, yang berisi air ( Gambar 1A ). Pemanasan peralatan membantu sirkulasi bahan awal dan bertujuan untuk meniru penguapan dalam sistem Bumi purba. Kedua, protokol yang dijelaskan di sini merekomendasikan siklus hidup/mati 1 jam saat menggunakan kumparan Tesla, yang secara efektif menggandakan waktu yang dibutuhkan untuk menyelesaikan eksperimen, dibandingkan dengan eksperimen yang dilakukan oleh Miller, karena ia terus menerus melepaskan listrik ke dalam sistem⁴ . Ketiga, karena generator percikan api tidak dimaksudkan untuk penggunaan jangka panjang, generator tersebut rentan terhadap kerusakan selama penggunaan yang berkepanjangan dan harus dirawat secara teratur dan terkadang diganti dengan unit cadangan, jika generator percikan api utama gagal selama eksperimen. Terakhir, protokol yang dijelaskan di sini melibatkan penggunaan keran kaca, yang membutuhkan gemuk vakum tinggi untuk membuat segel yang sesuai. Jika diinginkan, keran politetrafluoroetilena (PTFE) dapat digunakan untuk menghindari gemuk vakum. Namun, jika memeriksa keran ini untuk potensi kebocoran dengan detektor kebocoran percikan api, berhati-hatilah agar tidak terlalu memaparkan PTFE ke percikan api karena hal ini dapat mengganggu integritas PTFE dan menyebabkan segel yang buruk yang dibuat oleh keran ini.
Signifikansi metode yang dilaporkan di sini sehubungan dengan teknik yang ada, terletak pada kesederhanaannya. Metode ini menggunakan labu 3 L yang tersedia secara komersial, yang juga jauh lebih tahan lama dan lebih mudah dibersihkan di antara percobaan daripada desain asli yang digunakan oleh Miller 5. Karena peralatannya kurang rumit, ukurannya cukup kecil untuk melakukan percobaan di dalam lemari asam.
Setelah teknik yang diuraikan di sini dikuasai, teknik ini dapat dimodifikasi dengan berbagai cara untuk mensimulasikan berbagai jenis lingkungan terestrial primitif. Misalnya, campuran gas yang lebih teroksidasi dapat digunakan 14,18,19 . Lebih lanjut, dengan menggunakan modifikasi peralatan, sumber energi dapat diubah, misalnya, dengan menggunakan pelepasan diam 4 , sinar ultraviolet 20 , mensimulasikan sistem vulkanik 4,12,21 , meniru radioaktivitas dari kerak bumi 22 , dan meniru energi yang dihasilkan oleh gelombang kejut dari dampak meteorit 23 , dan juga radiasi kosmik 18,19 .
Eksperimen klasik Miller-Urey menunjukkan bahwa asam amino, blok pembangun penting protein biologis, dapat disintesis menggunakan bahan awal sederhana dalam kondisi terestrial prabiotik yang disimulasikan. Eksitasi molekul gas oleh lucutan listrik menyebabkan produksi senyawa organik, termasuk asam amino, dalam kondisi tersebut. Meskipun asam amino penting untuk biologi kontemporer, eksperimen Miller-Urey hanya memberikan satu mekanisme yang mungkin untuk sintesis abiotiknya, dan tidak menjelaskan asal usul kehidupan, karena proses yang menghasilkan organisme hidup kemungkinan lebih kompleks daripada pembentukan molekul organik sederhana.
Pengungkapan
Para penulis menyatakan tidak memiliki kepentingan finansial yang bersaing.
Ucapan Terima Kasih
Penelitian ini didukung bersama oleh Program Astrobiologi NSF dan NASA, di bawah Pusat Evolusi Kimia NSF, CHE-1004570, dan Pusat Astrobiologi Goddard. ETP ingin mengucapkan terima kasih atas pendanaan tambahan yang diberikan oleh Program Magang Biologi Planet NASA. Para penulis juga ingin berterima kasih kepada Dr. Asiri Galhena atas bantuan yang sangat berharga dalam menyiapkan fasilitas laboratorium awal.
Referensi
- Oparin AI. Asal Usul Kehidupan. Izd. Moskovshii Rabochii; 1924. [ Google Cendekia ]
- Haldane JB. Asal usul kehidupan. Rationalist Annu. 1929;148:3–10. [ Google Scholar ]
- Garrison WM, Morrison DC, Hamilton JG, Benson AA, Calvin M. Pengurangan Karbon Dioksida dalam Larutan Berair dengan Radiasi Ionisasi. Sains. 1951;114:416–418. doi: 10.1126/science.114.2964.416. [ DOI ] [ PubMed ] [ Google Scholar ]
- Miller SL. Produksi Beberapa Senyawa Organik di Bawah Kemungkinan Kondisi Bumi Primitif. J. Am. Chem. Soc. 1955;77:2351–2361. [ Google Scholar ]
- Miller SL. Produksi Asam Amino di Bawah Kondisi Bumi Primitif yang Mungkin Terjadi. Sains. 1953;117:528–529. doi: 10.1126/science.117.3046.528. [ DOI ] [ PubMed ] [ Google Scholar ]
- Heyns HK, Walter W, Meyer E. Percobaan model tentang pembentukan senyawa organik dalam atmosfer gas sederhana melalui lucutan listrik (Diterjemahkan dari bahasa Jerman) Die Naturwissenschaften. 1957;44:385–389. [ Google Scholar ]
- Ponnamperuma C, Woeller F. α-Aminonitriles yang terbentuk akibat lucutan listrik melalui campuran metana anhidrat dan amonia. Biosystems. 1967;1:156–158. doi: 10.1016/0303-2647(67)90031-7. [ DOI ] [ PubMed ] [ Google Scholar ]
- Oró J. Sintesis Senyawa Organik dengan Pelepasan Listrik. Alam. 1963;197:862–867. [ Google Scholar ]
- Ring D, Wolman Y, Friedmann N, Miller SL. Sintesis Prebiotik Asam Amino Hidrofobik dan Protein. Proc. Natl. Acad. Sci. USA 1972;69:765–768. doi: 10.1073/pnas.69.3.765. [ DOI ] [ Artikel PMC gratis ] [ PubMed ] [ Google Scholar ]
- Wolman Y, Haverland WJ, Miller SL. Asam Amino Nonprotein dari Pelepasan Percikan dan Perbandingannya dengan Asam Amino Meteorit Murchison. Proc. Natl. Acad. Sci. USA 1972;69:809–811. doi: 10.1073/pnas.69.4.809. [ DOI ] [ Artikel PMC gratis ] [ PubMed ] [ Google Scholar ]
- Roscoe S, Miller SL. Hasil Energi untuk Sintesis Hidrogen Sianida dan Formaldehida: Konsentrasi HCN dan Asam Amino di Lautan Primitif. Orig. Life. 1987;17:261–273. doi: 10.1007/BF02386466. [ DOI ] [ PubMed ] [ Google Scholar ]
- Johnson AP, dkk. Eksperimen Pelepasan Percikan Api Vulkanik Miller. Sains. 2008;322 doi: 10.1126/science.1161527. [ DOI ] [ PubMed ] [ Google Scholar ]
- Parker ET, dkk. Sintesis primordial amina dan asam amino dalam eksperimen lucutan percikan kaya H2S Miller tahun 1958. Proc. Natl. Acad. Sci. USA 2011;108:5526–5531. doi: 10.1073/pnas.1019191108. [ DOI ] [ Artikel PMC gratis ] [ PubMed ] [ Google Scholar ]
- Cleaves HJ, Chalmers JH, Lazcano A, Miller SL, Bada JL. Penilaian ulang sintesis organik prebiotik di atmosfer planet netral. Orig. Life Evol. Biosph. 2008;38:105–115. doi: 10.1007/s11084-007-9120-3. [ DOI ] [ PubMed ] [ Google Scholar ]
- Glavin DP, dkk. Analisis asam amino meteorit CM2 Antartika menggunakan kromatografi cair-spektrometri massa waktu terbang. Meteorit. Planet. Sci. 2006;41:889–902. [ Google Scholar ]
- Zhao M, Bada JL. Penentuan asam α-dialkilamino dan enantiomernya dalam sampel geologi dengan kromatografi cair kinerja tinggi setelah derivatisasi dengan aduk kiral o-ftaldialdehida. J. Chromatogr. A. 1995;690:55–63. doi: 10.1016/0021-9673(94)00927-2. [ DOI ] [ PubMed ] [ Google Scholar ]
- Strecker A. Tentang pembentukan asam laktat buatan dan glikokol baru, badan homolog Justus Liebigs Annalen der Chemie. 1850;75:27–45. [ Google Scholar ]
- Miyakawa S, Yamanashi H, Kobayashi K, Cleaves HJ, Miller SL. Sintesis prebiotik dari atmosfer CO: implikasi bagi asal usul kehidupan. Proc. Natl. Acad. Sci. USA 2002;99:14628–14631. doi: 10.1073/pnas.192568299. [ DOI ] [ Artikel PMC gratis ] [ PubMed ] [ Google Scholar ]
- Kobayashi K, Kaneko T, Saito T, Oshima T. Pembentukan Asam Amino dalam Campuran Gas oleh Iradiasi Partikel. Orig. Life Evol. Biosph. 1998;28:155–165. doi: 10.1023/a:1006561217063. [ DOI ] [ PubMed ] [ Google Scholar ]
- Sagan C, Khare BN. Fotoproduksi Asam Amino dengan Sinar Ultraviolet Gelombang Panjang di Bumi Purba. Sains. 1971;173:417–420. doi: 10.1126/science.173.3995.417. [ DOI ] [ PubMed ] [ Google Scholar ]
- Harada K, Fox SW. Sintesis Termal Asam Amino Alami dari Atmosfer Bumi Primitif yang Diduga Ada. Nature. 1964;201:335–336. doi: 10.1038/201335a0. [ DOI ] [ PubMed ] [ Google Scholar ]
- Ponnamperuma C, Lemmon RM, Mariner R, Calvin M. Pembentukan Adenin melalui Iradiasi Elektron Metana, Amonia, dan Air. Proc. Natl. Acad. Sci. USA. 1963;49:737–740. doi: 10.1073/pnas.49.5.737. [ DOI ] [ Artikel PMC gratis ] [ PubMed ] [ Google Scholar ]
- Bar-Nun A, Bar-Nun N, Bauer SH, Sagan C. Sintesis Asam Amino secara Mendadak dalam Lingkungan Primitif yang Disimulasikan. Sains. 1970;168:470–473. doi: 10.1126/science.168.3930.470. [ DOI ] [ PubMed ] [ Google Scholar ]



Comments
Post a Comment